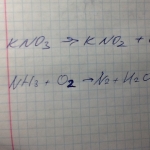Окислительно-восстановительные реакции
5-9 класс|
|
________________________________
2KNO3--->2KNO2+O2
2K(+1)N(+5)O3(-2)--->2K(+1)N(+3)O2(-2)+O2(0)
2| N(+5) + 2e->N(+3) (окисление)
2 | O(-2) - 2e->O2(0) (восстановление)
KNO3-восстановитель ,О2- окислитель
____________________________________
4NH3 +5O2--->4NO + 6 H2O
4N(-3)H3(+1) +5O2(0)---> 4N(+2)O(-2) + 6 H2(-1)O(-2)
4| N(-3) - 5e -> N(+2) (окисление )
5| O2(0) + 4e -> 2O(-2) (восстановление )
NH3-восстановитель ,О2-окислитель
Другие вопросы из категории
Читайте также
и восстановления:
1. P + HNO3 + H2O = H3PO4 + NO
2. P + HNO3 = H3PO4 + NO2 + H2O
3. K2Cr2O7 + HCl = Cl2 + KCl + CrCl3 + H20
4. KMnO4 + H2S + H2SO4 = MnSO4 + S + K2SO4 + H2O
5. KMnO4 + HCl = Cl2 + MnCl2 + KCl + H2O
Методом электронного баланса подберите коэффициенты в схемах окислительно-восстановительных реакций и укажите процесс окисления и восстановления:
CuO+ NH3= Cu + N2 +H2O
Ag +HNO3 = AgNO3 + NO +H2O
Zn + HNO3= Zn (NO3)2 + N2 + H2O
Cu +H2SO4= CuSO4 +SO2 +H2O
Fe+CuSO4 -
решить как окислительно-восстановительные реакция
и как - реакция ионного обмена
+H2=Cu+H2O
2) SiO2 + 2NaOH= Na2SiO3 + H2O
3) CaO + H2O=Ca(OH)2
4) 2NO +O2=2NO2
Укажите, какие из привeденных уравнений относятся к окислительно-восстановительным реакциям:
1) 2NaBr +Cl2 + 2NaCl2=2NaCl + Br2
2) SiO2 +2MgO=Si+2MgO
3) 4NH3 +3O2 + 2N2 + 6H2O
4) Mg (OH)2 +H2SO4=MgSO4 +2H2O
ПОЖАЛУЙСТА! МНЕ ОЧЕНЬ ПРИ ОЧЕНЬ СРОЧНО НАДО, ЛУЧШЕ СФОТОГРАФИРОВАТЬ, А ТО Я СОВСЕМ ТЕМУ НЕ ПОНЯЛА- БОЛЕЛА. пОМОГИТЕ МНЕ РЕШИТЬ РАСПИШИТЕ ПОЖАЛУЙСТА!!! уМОЛЯЮ!! НУЖНА ПОМОЩЬ!! СРРОООЧНО
6)PbO+H2=
расставьте коэффициенты в уравнениях окислительно-восстановительных реакций:
1) H2S+Cl2=HCl+S
2)HNO3+Cu=Cu(NO3)2+NO2+H2O
3)HCl+MnO2=MnCl2+H2O+Cl2 помогите пожалуйста очень прошу)
УРАВНЕНИЯМИ РЕАКЦИЙ И РАССМОТРИТЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ, ИСПОЛЬЗУЯ МЕТОД ЭЛЕКТРОННОГО БАЛАНСА.
 сервис вопросов и ответов
сервис вопросов и ответов