не могу понять как решить, помогите пожалуйста: вычислить массу серебра, которая выделиться при реакции "серебряного зеркала", если практический выход
10-11 класс|
|
серебра 80% от теоретически возможного, если в реакцию вступило 10 грамм раствора формалина.
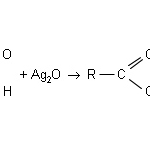
вместо "R" "H"
HCHO+Ag2O=HCOOH+2Ag
n(HCHO)=10/30=0.33 моль
Mr(HCHO)=30
по уравнению реакции на 1 моль HCHO приходится 2 моль Ag
следовательно n(Ag)=0.33*2=0.66 моль Ar(Ag)=108
m(Ag)=108*0.66=71.28г теоретически 100% выход
находим практическую массу серебра
m(Ag)=71.2*0.8=57 г
n(CH2O) = 10/30 = 0,33 моль
n(Ag) = 0,33*2 = 0,66 моль - теоретическая
n(Ag) = 0,8*0,66 = 0,528 моль - практическая
m(Ag) = 0,528*108 = 57 г
Другие вопросы из категории
Читайте также
1. В результате взаимодействия кальций гидроксида массой 37 г с амоний сульфатом получили 15 г амониака. Вычислите массовую долю выхода амониака.
2. Вычислите объем амониака (н. у.), который можно получить в результате взаимодействия амоний хлорида массой 30 г с избытком кальций гидроксида, принимая, что объемная доля выхода амониака составляет 92%.
Помогите пожалуйста! Очень надо.. . Буду очень-очень благодарна, если хоть одну напишите.. . Спасибо
1)
на 26,75 г аммоний хлорида подействовали раствором содержащий 16 г
гидроксида натрия. Какой объем аммиака при этом задействовали?
2) вычислите объем водорода, который выделится при взаимодействии цинка массой 13 г с раствором, содержащим 49 г серной кислоты.
3) Вычислить массу соли, которая образуется при взаимодействии 10,2 г аммиака с азотной кислотой массой 37,8 г.
4)
Вычислите массу соли, образовавшейся при взаимодействии 64 г гидроксида
натрия с раствором серной кислоты, содержащий 19,6 г H2SO4
Не могу понять какое из этих уравнений реакции составлено верно, а какое не верно ?
Ca+2H2O=Ca(OH)2+2H И
насыщенный при 20 С раствор медного купорос содержит 27% 5-водного сульфата меди 2 (плотность 1.2 г/мл) . При какой силе тока можно в течение 3 часов выделить всю медь из 1л такого раствора?
 сервис вопросов и ответов
сервис вопросов и ответов