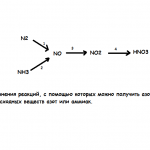
1. Составьте уравнения реакций, с помощью которых можно получить азотную кислоту, взяв в качестве исходных веществ азот или
5-9 класс|
|
аммиак.
(Задание в прикрепленном файле.)
2. Расставьте методом электронного баланса коэффициенты в реакциях, схемы которых:
а) HNO3(конц)+Cu---> NO2+H2O
б) HNO3(разб)+СU---> Cu(NO3)2+NO+H2O
в) HNO3(разб)+Al---> Al(NO3)3+N2O+H2O
г) HNO3(разб)+Mg---> Mg(NO3)2+NO2+H2O
1.1)N2+O2=2NO;2)NO+H2O+No2+H2;3)NO2+H2O=HNO3
1)4NH3+5O2=4No+6H2O;2)NO+H2O+NO2+H2;3)NO2+H2O=HNO3
2)
1.N2+O2=2NO (высокая температура, катализатор, или грозовой разряд)
4NH3+5O2=4NO+6H2O (высокая температура, катализатор, высокое давление)
(как правило, а промышленности используется второй способ, катализаторы - платина Pt или пентаоксид диванадия - V2O5)
2NO+O2=2NO2 (высокая температура)
4NO2+4H2O+O2=4HNO3
2. (по-моему, вы пропустили нитрат меди (Cu(NO3)2) в первом уравнении):
метод электронного баланса основан на том, что элементы обмениваются электронами (т.е. электроны не появляются ниоткуда и не исчезают в никуда), поэтому, вам нужно:
1) подсчитать степени окисления всех элементов
2) найти элементы с изменяющимися степенями окисления
3) посчитать количество электронов, которые отдает восстановитель и принимает окислитель
4) расставить коэффициенты для этих элементов так, чтобы количество электронов отдаваемых и принимаемых было одинаково
5) все остальные элементы уравнять
а) 4HNO3+Cu=Cu(NO3)2+2NO2+2H2O
смотрите, медь из степени окисления 0 переходит в состояние +2, т.е. отдает 2 электрона, а азот принимает 1 электрон ( с +5 до +4), значит, на каждый атом меди должно быть два атома азота. Это записывается так:
Cu(0) -2e ->Cu(+2) /1
N(+5) +1e ->N(+4) /2
б,в,г попробуйте сами:
б) 3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O
в)8Al+30HNO3=8Al(NO3)3+3N2O+15H2O
г)Mg+4HNO3=Mg(NO3)2+2NO2+2H2O (вы уверены, что в г кислота разбавлена и получается NO2?)
(Есть еще метод электронно-ионного баланса, но о нем в следующий раз).
Другие вопросы из категории
сроччноооооооооооо
_Ca(OH)2+_CO2=
_Ca(OH)2+_SO2=
_NaOH+_SO3=
_Ca(OH)2+_SiO2=
_NaOH+_P2O5=
_NaOH+_SiO2=
_NaOH+_N2O5=
_Ca(OH)2+_N2O5=
Читайте также
/p>
2. Напишите уравнения реакций, с помощью которых можно осуществить цепочку превращений веществ: Хлорид натрия - Натрий - Сульфид натрия - Сульфат натрия - Нитрат натрия
3. Напишите уравнения возможных реакций между аллюминием и веществом из следующего перечня: кислород, сера, хлор, вода, серная разбавленная кислота, гидроксид натрия, хлорид ртути (||). Ко всем уравнениям составьте схему электронного баланса или схематически обозначьте степени окисления и переход электронов
уравнения реакций, с помощью которых можно осуществить цепочку превращения веществ:
а) Натрий -> Гидроксид натрия -> Нитрат натрия
б) Калий -> Гидроксид калия -> Карбонат калия
в) Медь -> Оксид меди(II) -> Гидроксид меди (II) -> Оксид меди (II)
концентрированной и неконцентрированной азотной кислотой
в)составить уравнения реакций меди с концентрированной и неконцентрированной азотной кислотой
+HCl
Si→Mg2Si → SiH4→SiO2 →Si
2)
В трех пронумерованных пробирках находятся растворы солей карбоната калия, йодида калия и сульфата калияю Напишите уравнения реакций, с помощью которых опытным путем их можно распознатью
3)
При длительном пропускании углекислого газа через известковую воду образуется осадок, который затем исчезает. Напишите уравненя соответсвующих реакций.
4)
При сгорании 187.5 г угля образовалось 336 л оксида углерода (4) (н.у.). Вычислите массовую долю углерода в угле.
Al4C3
2)Составьте уравнения реакций,подберите коэффициенты для следующих схем превращений:
1.Al2O3 -
AlO2 -
2.Al(OH)3 -
- Al
3.[Al(OH)4] -
[Al(OH)4(H2O)2] -
 сервис вопросов и ответов
сервис вопросов и ответов