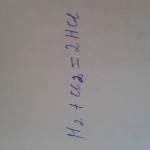составить электронный баланс
10-11 класс|
|
ПОМОГИТЕ ПОЖАЛУЙСТА
2H^0 - 2e -> 2H^+ восстановитель
2Cl^0 + 2e -> 2Cl^- окислитель
H(0)2+Cl(0)2=H(+)Cl(-)
2H(0)-2e-=2H(+) 1- восстановитель
2Cl(0)+2e-=2Cl(-) 1 - окислитель
2H(0)+2Cl(0)=2H(+)+2Cl(-)
H2+Cl2=2HCl
Другие вопросы из категории
Читайте также
HBrO3 + H2S → S + Br2 + H2O
Определите окислитель и восстановитель.
2.
Используя метод электронного баланса, составьте уравнение реакции
Zn + HNO3 → Zn(NO3)2 + N2O + H2O
Определите окислитель и восстановитель.
3.
В реакции, схема которой
CuO + NH3 → Cu + N2 + H2O,
окислителем является
1)Сu0
2)N-3
3)О-2
4)Сu+2
определение понятиям окисление и восстановление.
32. Используя метод электронного баланса, составьте уравнение реакции: K2Cr2O7 + KI + H2SO4 = I2 + Cr2(SO4)3 + K2SO4 +H2O
окислитель и восстановитель. 2)Используя метод электронного баланса, составьте уравнение реакции: FeSO4+K2Cr2O7+...---> ... + Cr2(SO4)3+... + H2O Определите окислитель и восстановитель.
коэффициенты!KMnO4+Na2SO3+H2O->.............+Na2SO4+KOH
Электронный баланс
Для 1, 4 реакции составьте электронный баланс
 сервис вопросов и ответов
сервис вопросов и ответов