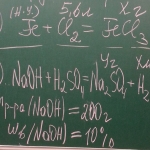Помогите срочно! Пожалуйста !
5-9 класс|
|
1) 2Fe + 3Cl2 = 2FeCl3
Рассчитаем количество вещества хлора:
n= V/Vm = 5,6л/22,4л/моль = 0,25 моль
по уравнению реакции:
n(FeCl3) = 2/3n(Cl2) = 0,167 моль
m(FeCl3) = n*M = 0,167 моль*162,5 г/моль = 27,1375 г
Ответ: m(FeCl3) = 27,1375 г
2) 2NaOH + H2SO4 = Na2SO4 + 2h2O
Рассчитаем массу гидроксида натрия в растворе:
m(NaOH) = w*m(р-ра) = 0,1*200г = 20г
Рассчитаем количество вещества гидроксида натрия:
n = m/M = 20г/40г/моль = 0,5 моль
По уравнению реакции:
n(Na2SO4) = 1/2n(NaOH) = 0,25 моль
По уравнению реакции:
n(H2O) = n(NaOH) = 0,5 моль
Рассчитаем массу сульфата:
m = n*M = 0,25 моль*142 г/моль = 35,5 г
Ответ: m(Na2SO4) = 35,5г
n(H2O) = 0,5 моль
Другие вопросы из категории
Читайте также
Вычислите объем углекислого газа,выделившегося при действии избытка соляной кислоты на 50г мела,содержащего 3% некарбонатных примесей.
ОЧЕНЬ СРОЧНО ПОЖАЛУЙСТА ПОМОГИТЕ!!!!
классификации элементов " пожалуйста помогите срочно пожалуйста пожалуйста пожалуйста пожалуйста...
1. 7 г. цинка взаимодействует с соляной кислотой. Рассчитать массу образовавшиеся соли и обьём выделившегося водорода
2 ВО ВЛОЖЕНИИ! ТАМ НАДО НАПИСАТЬ РЕАКЦИИ И УКАЗАТЬ ИХ ТИПЫ! ПОМОГИТЕ СРОЧНО ПЛИЗ!!!!!
помогите срочно!!!!
написать уравнения реакции:
а) гидроксид лития и азотная кислота
б) нитрат меди (II) и гидроксид натрия
в) карбонат калия и фосфорная кислота
1.10 г. серной кислоты вступило в реакцию с гидроксидом натрия в реакцию нейтрализации. Рассчитать массу образовавшиеся соли.
2. 7 г. цинка взаимодействует с соляной кислотой. Рассчитать массу образовавшиеся соли и обьём выделившегося водорода.
3, S-SO4-SO3-HCL-NA3SO4 ДАЛЬШЕ ПОД SO4 СТРЕЛКА ВНИЗ H2SO3-MGSO3
НУЖНО УКАЗАТЬ ТИПЫ РЕАКЦИЙ ПЛИЗ ПОМОГИТЕ СРОЧНО!!! ЗАРАНЕЕ БЛАГОДАРЮ!!!
 сервис вопросов и ответов
сервис вопросов и ответов