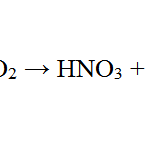Составьте на основе электронного баланса полные уравнения реакции, указав окислитель и восстановитель:
10-11 класс|
|
N(+3)-2e=N(+5) восстановитель
N(+3)+1e=N(+2) окислитель
3HNO2=HNO3 + 2NO + H2O
Другие вопросы из категории
Нужно очень срочно
а) реагирует с активными металлами
б) образует соли с основными гидроксидами
в) образует соли с амфотерными оксидами
г) окисляет малоактивные металлы с выделением хлора
д) восстанавливает перманганат калия
Читайте также
H2S+H2SO3=S+H2O
KMnO4+NaNO2=H2O=MnO2=NaNO3+KOH
барий->сульфид бария->хлорид бария->барий->оксид бария->сульфат бария
Для одной окислительно-восстановительной реакции составьте электронный баланс,для одной реакции ионного обмена напишите полное и сокращенное ионное уравнения.
указать окислитель и восстановитель.
2)Осуществить превращения реакций: Zn→ZnO→ZnCl2→Zn(OH)2 Рассмотрите ОВР. Запишите ионные уравнения реакций, где возможно.
восстановления .
Реакция
Na2MnO4+H2O --> MnO2+NaMnO4+NaOH
 сервис вопросов и ответов
сервис вопросов и ответов